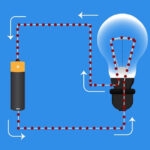
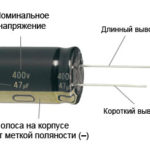
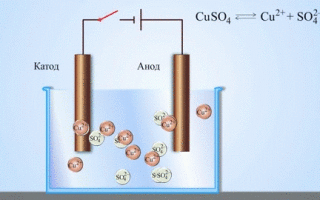
Često postoji problem određivanja koja od elektroda je katoda, a koja anoda. Prvo morate razumjeti pojmove.
Sadržaj
Koncept katode i anode - jednostavno objašnjenje
U složenim tvarima elektroni su neravnomjerno raspoređeni između atoma u spojevima. Kao rezultat interakcije, čestice se kreću od atoma jedne tvari do atoma druge. Reakcija se naziva redoks. Gubitak elektrona naziva se oksidacija, a element koji donira elektrone naziva se redukcijski agens.
Dodavanje elektrona naziva se redukcija, element primanja u ovom procesu je oksidacijsko sredstvo. Prijenos elektrona s redukcijskog sredstva na oksidacijsko sredstvo može se odvijati kroz vanjski krug, a zatim se može koristiti kao izvor električne energije.Uređaji u kojima se energija kemijske reakcije pretvara u električnu energiju nazivaju se galvanske ćelije.
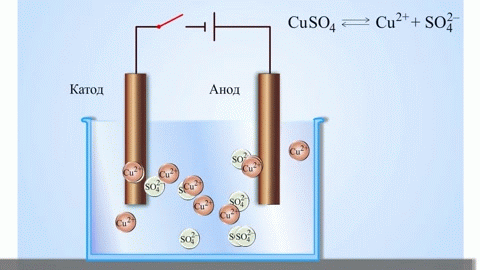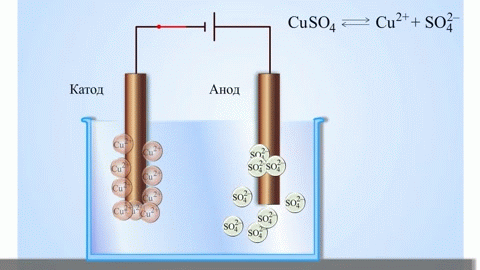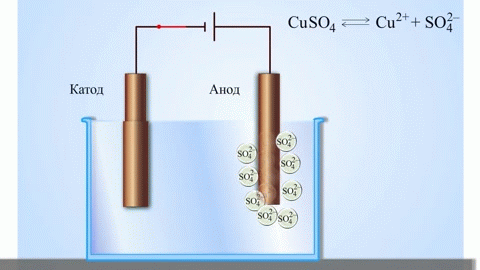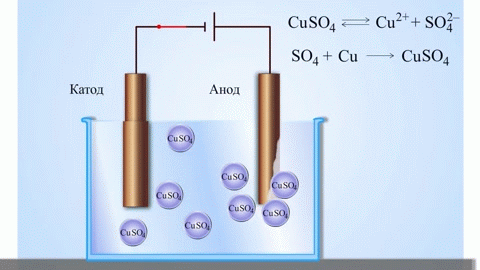
Najjednostavniji klasični primjer galvanske ćelije su dvije ploče izrađene od različitih metala i uronjene u otopinu elektrolita. U takvom sustavu oksidacija se događa na jednom metalu, a redukcija na drugom.
VAŽNO! Elektroda na kojoj dolazi do oksidacije naziva se anoda. Elektroda na kojoj se vrši redukcija je katoda.
Iz školskih udžbenika kemije poznat je primjer bakreno-cink galvanske ćelije koja radi zahvaljujući energiji reakcije između cinka i bakrenog sulfata. U uređaju Jacobi-Daniel bakrena ploča se stavlja u otopinu bakrenog sulfata (bakrena elektroda), cink ploča se uroni u otopinu cink sulfata (cinkova elektroda). Cinkova elektroda ispušta katione u otopinu, stvarajući u njoj višak pozitivnog naboja, a na bakrenoj elektrodi otopina se iscrpljuje kationima, ovdje je otopina negativno nabijena.
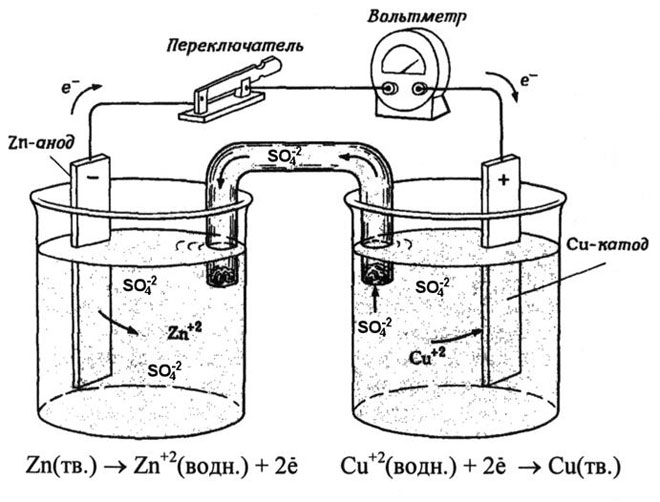
Zatvaranje vanjskog kruga uzrokuje strujanje elektrona od cink elektrode do bakrene elektrode. Ravnotežni odnosi na granicama faza su prekinuti. Događa se oksidacijsko-redukcijska reakcija.
Energija spontane kemijske reakcije pretvara se u električnu energiju.
Ako je kemijska reakcija izazvana vanjskom energijom električne struje, odvija se proces koji se naziva elektroliza. Procesi koji se odvijaju tijekom elektrolize obrnuti su od procesa koji se događaju tijekom rada galvanske ćelije.
PAŽNJA! Elektroda na kojoj se odvija redukcija naziva se i katoda, ali je u elektrolizi negativno nabijena, dok je anoda pozitivno.
Primjena u elektrokemiji
Anode i katode sudjeluju u mnogim kemijskim reakcijama:
- Elektroliza;
- Elektroekstrakcija;
- galvanizacija;
- Elektrotipija.
Metali se dobivaju elektrolizom rastaljenih spojeva i vodenih otopina, metali se pročišćavaju od nečistoća i ekstrahiraju vrijedne komponente (elektrolitičko rafiniranje). Ploče se lijevaju od metala koji se čisti. Postavljaju se kao anode u elektrolizer. Pod utjecajem električne struje metal se otapa. Njegovi kationi prelaze u otopinu i ispuštaju se na katodi, stvarajući talog čistog metala. Nečistoće sadržane u izvornoj neočišćenoj metalnoj ploči ili ostaju netopive kao anodni mulj ili prelaze u elektrolit gdje se uklanjaju. Bakar, nikal, olovo, zlato, srebro, kositar podvrgnuti su elektrolitičkoj rafinaciji.
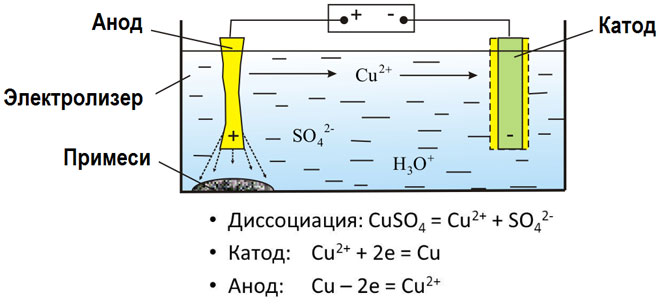
Elektroekstrakcija je proces odvajanja metala iz otopine tijekom elektrolize. Kako bi metal otišao u otopinu, obrađuje se posebnim reagensima. Tijekom procesa na katodi se taloži metal visoke čistoće. Tako se dobiva cink, bakar, kadmij.
Kako bi se izbjegla korozija, dala čvrstoća, ukrasila proizvod, površina jednog metala prekrivena je slojem drugog. Taj se proces naziva galvanizacija.

Galvanizacija je postupak dobivanja metalnih kopija iz rasutih predmeta elektrotaloženjem metala.

Primjena u vakuumskim elektroničkim uređajima
Princip rada katode i anode u vakuumskom uređaju može se pokazati elektronskom lampom.Izgleda kao hermetički zatvorena posuda s metalnim dijelovima unutra. Uređaj se koristi za ispravljanje, generiranje i pretvaranje električnih signala. Prema broju elektroda razlikuju se:
- diode;
- triode;
- tetrode;
- pentode itd.
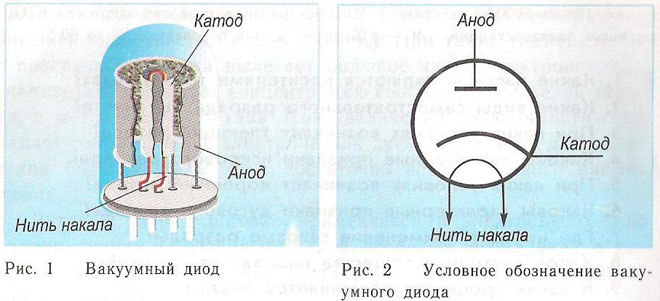
Dioda je vakuumski uređaj s dvije elektrode, katodom i anodom. Katoda je spojena na negativni pol izvora napajanja, anoda - na pozitivni. Svrha katode je emitiranje elektrona kada se zagrije električnom strujom do određene temperature. Emitirani elektroni stvaraju prostorni naboj između katode i anode. Najbrži elektroni jure prema anodi, prevladavajući negativnu potencijalnu barijeru prostornog naboja. Anoda prima te čestice. U vanjskom krugu stvara se anodna struja. Elektroničkim protokom upravljaju dodatne elektrode primjenom električnog potencijala na njih. Pomoću dioda izmjenična struja se pretvara u istosmjernu.
Primjena u elektronici
Danas se koriste poluvodičke vrste dioda.
U elektronici se široko koristi svojstvo dioda da struju propuštaju u smjeru naprijed i da ne prolaze u suprotnom smjeru.
Rad LED-a temelji se na svojstvu poluvodičkih kristala da svijetle kada struja prolazi kroz p-n spoj u smjeru naprijed.
Galvanski izvori istosmjerne struje - baterije
Kemijski izvori električne struje u kojima se odvijaju reverzibilne reakcije nazivaju se baterije: pune se i više puta koriste.

Tijekom rada olovne baterije dolazi do redoks reakcije.Metalno olovo oksidira, donira svoje elektrone, reducira olovni dioksid, koji prihvaća elektrone. Olovni metal u bateriji je anoda i negativno je nabijen. Olovni dioksid je katoda i pozitivno je nabijen.
Kako se baterija prazni, troše se tvari katode i anode i njihov elektrolit, sumporna kiselina. Za punjenje baterije spojen je na izvor struje (plus na plus, minus na minus). Smjer struje sada je obrnut od onoga kada je baterija bila prazna. Elektrokemijski procesi na elektrodama su "obrnuti". Sada olovna elektroda postaje katoda, na njoj se odvija proces redukcije, a olovni dioksid postaje anoda, pri čemu se odvija postupak oksidacije. Baterija ponovno stvara tvari potrebne za njezin rad.
Zašto dolazi do zabune?
Problem proizlazi iz činjenice da se određeni znak naboja ne može čvrsto pričvrstiti na anodu ili katodu. Često je katoda pozitivno nabijena elektroda, a anoda negativna. Često, ali ne uvijek. Sve ovisi o procesu koji se odvija na elektrodi.
PAŽNJA! Dio koji se stavlja u elektrolit može biti i anoda i katoda. Sve ovisi o svrsi postupka: trebate staviti još jedan sloj metala na njega ili ga ukloniti.
Kako prepoznati anodu i katodu
U elektrokemiji, anoda je elektroda na kojoj se odvijaju procesi oksidacije, katoda je elektroda na kojoj dolazi do redukcije.
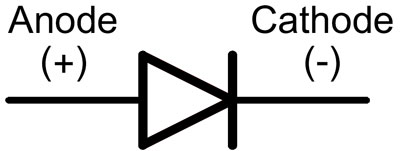
U diodi se slavine nazivaju anoda i katoda. Struja će teći kroz diodu ako je anodna slavina spojena na "plus", "katodna" slavina - na "minus".
Za novu LED diodu s nerezanim kontaktima, anoda i katoda se vizualno određuju duljinom. Katoda je kraća.

Ako su kontakti odsječeni, pomoći će baterija koja je na njih pričvršćena. Svjetlo će se pojaviti kada se polariteti podudaraju.
Znak anoda i katode
U elektrokemiji je ispravnije govoriti ne o znakovima naboja elektroda, već o procesima koji se odvijaju na njima. Reakcija redukcije se odvija na katodi, a reakcija oksidacije na anodi.
U elektrotehnici, za protok struje, katoda je spojena na negativni pol izvora struje, anoda na pozitivni.
Slični članci: